Adenosiintrifosfaat või ATP Kuna organism on energiarikkaim molekul, vastutab ta kõigi energiat ülekandvate protsesside eest. See on puriini aluse adeniini mononukleotiid ja seetõttu ka nukleiinhapete komponent.ATP sünteesi häired pärsivad energia vabanemist ja põhjustavad kurnatuse.
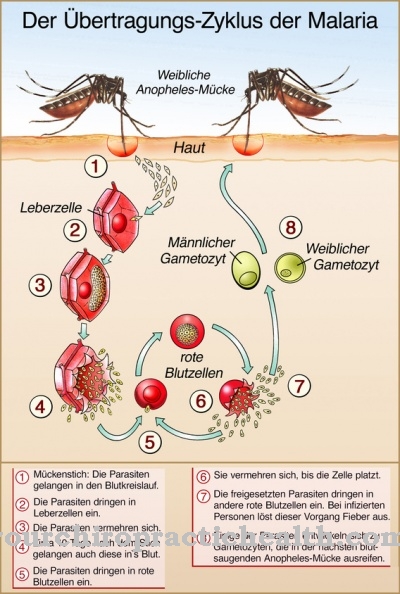
Mis on adenosiintrifosfaat?
Adenosiintrifosfaat (ATP) on adeniini mononukleotiid, millel on kolm fosfaatrühma, mis on üksteisega ühendatud anhüdriidsideme kaudu. ATP on keskne molekul energia edastamiseks organismis.
Energia seondub peamiselt beetafosfaatjäägi anhüdriidsidemes gammafosfaadijäägiga. Kui adenosindifosfaadi moodustumisel eemaldatakse fosfaatjääk, vabaneb energia. Seejärel kasutatakse seda energiat energiat tarbivateks protsessideks. Nukleotiidina koosneb ATP puriini aluse adeniinist, suhkru riboosist ja kolmest fosfaatjäägist. Adeniini ja riboosi vahel on glükosiidside. Lisaks on alfafosfaatjääk riboosiga seotud estersidemega.
Alfa-beeta ja gammafosfaadi vahel on anhüdriidside. Pärast kahe fosfaadi eemaldamist moodustub nukleotiid-adenosiinmonofosfaat (AMP). See molekul on RNA oluline ehitusplokk.
Funktsioon, mõju ja ülesanded
Adenosiintrifosfaadil on organismis mitmesuguseid funktsioone. Selle peamine ülesanne on energia salvestamine ja ülekandmine. Kõik kehas toimuvad protsessid on seotud energiaülekannete ja energia muundamisega. Organism peab tegema keemilisi, osmootilisi või mehaanilisi töid. ATP annab kiiresti energiat kõigi nende protsesside jaoks.
ATP on lühiajaline energiasalv, mis on kiiresti ära kasutatud ja seetõttu tuleb seda uuesti ja uuesti sünteesida. Enamik energiat tarbivatest protsessidest on rakusisesed ja rakuvälised transpordiprotsessid. Biomolekulid transporditakse kohtadesse, kus nad reageerivad ja muunduvad. Anaboolsed protsessid, näiteks valkude süntees või keharasva moodustumine, vajavad ATP-d ka energiat edastava ainena.Molekulide transport rakumembraani või mitmesuguste rakuorganellide membraanide kaudu on samuti energiasõltuv.
Lisaks saab lihaste kontraktsioonide mehaanilist energiat kättesaadavaks teha ainult energiat tarnivast protsessist tuleneva ATP toimel. ATP on lisaks energiakandja funktsioonile ka oluline signaalmolekul. See toimib nn kinaaside kosubstraadina. Kinaasid on ensüümid, mis kannavad fosfaatrühmi teistesse molekulidesse. Peamiselt osalevad proteiinkinaasid, mis mõjutavad erinevate ensüümide aktiivsust erinevate ensüümide fosforüülimise kaudu. Rakuväliselt on ATP perifeerse ja kesknärvisüsteemi rakkude retseptorite agonist.
Seega osaleb ta verevoolu reguleerimisel ja põletikuliste reaktsioonide esilekutsumisel. Kui närvikoe on vigastatud, vabaneb see suuremates kogustes, et hõlbustada astrotsüütide ja neuronite suurenenud moodustumist.
Haridus, esinemine, omadused ja optimaalsed väärtused
Adenosiintrifosfaat on vaid lühiajaline energiavaru ja see kulub energiat tarbivates protsessides mõne sekundi jooksul. Seetõttu on selle pidev uuendamine ülioluline ülesanne. Molekulil on nii keskne roll, et ühel päeval toodetakse ATP massiga pool kehamassist. Adenosiindifosfaat muundatakse adenosiintrifosfaadiks täiendava sideme abil energiatarbimisega fosfaadiga, mis tarnib kohe energiat uuesti, lahustades fosfaadi ja muundades selle tagasi ADP-ks.
ATP regenereerimiseks on saadaval kaks erinevat reaktsiooniprintsiipi. Üks põhimõte on substraadi ahela fosforüülimine. Selles reaktsioonis kantakse fosfaatjääk energiat tarniva protsessi käigus otse vahemolekulile, mis kandub ATP moodustumisel kohe ADP-sse. Teine reaktsiooni põhimõte on hingamisahela osa elektronide transpordi fosforüülimisel. See reaktsioon toimub ainult mitokondrites. Selle protsessi käigus koguneb membraani kaudu mitmesuguste prootoneid transportivate reaktsioonide kaudu elektripotentsiaal.
Prootonite tagasivool põhjustab ATP moodustumist ADP-st koos energia eraldumisega. Seda reaktsiooni katalüüsib ensüüm ATP süntetaas. Üldiselt on need regenereerimisprotsessid mõne nõude jaoks endiselt liiga aeglased. Lihaste kontraktsiooni ajal kuluvad kõik ATP varud kahe kuni kolme sekundi pärast ära. Sel eesmärgil on lihasrakkudes saadaval energiarikas kreatiinfosfaat, mis muudab selle fosfaadi viivitamatult kättesaadavaks ATP moodustamiseks ADP-st. See varustus on nüüd kuue kuni kümne sekundi jooksul ammendunud. Pärast seda peavad üldised regenereerimisprotsessid uuesti kehtima. Kreatiinfosfaadi mõju tõttu on lihaste treenimist siiski võimalik pisut pikendada ilma enneaegse kurnatuseta.
Ravimid leiate siit
Fatigue Väsimuse ja nõrkuse ravimidHaigused ja häired
Kui adenosiintrifosfaati toodetakse liiga vähe, põhjustab see ammendumist. ATP sünteesitakse peamiselt mitokondrites elektronide transpordi fosforüülimise teel. Kui mitokondrite funktsioon on häiritud, väheneb ka ATP tootmine.
Uuringud on näidanud, et kroonilise väsimussündroomiga (CFS) patsientidel oli ATP kontsentratsioon vähenenud. See ATP vähenenud produktsioon korreleerus alati häiretega mitokondrites (mitokondriopaatiad). Mitokondriaalse haiguse põhjuste hulka kuulusid rakuline hüpoksia, EBV-ga seotud infektsioonid, fibromüalgia või kroonilised degeneratiivsed põletikulised protsessid. Mitokondrites on nii geneetilisi kui ka omandatud häireid. Kirjeldatud on umbes 150 erinevat haigust, mis põhjustavad mitokondriaalset haigust.
Nende hulka kuuluvad suhkurtõbi, allergiad, autoimmuunhaigused, dementsus, kroonilised põletikud ja immuunpuudulikkuse haigused. Nende haiguste kontekstis on kurnatusseisundid madalamad energiavarud ATP vähenenud tootmise tõttu. Selle tagajärjel võivad mitokondrite funktsiooni häired põhjustada mitmete elundite haigusi.


.jpg)









.jpg)