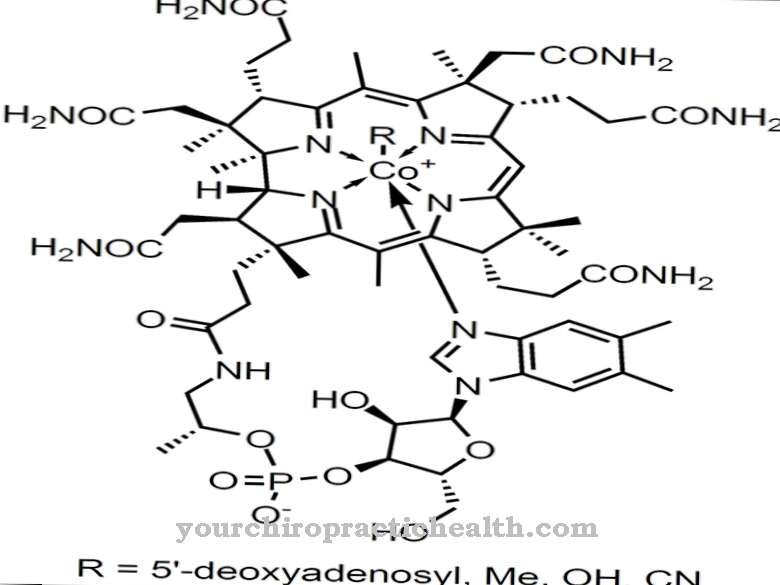
Fenüülalaniin "Proteinogeenne aminohape" on proteinogeenne asendamatu aminohape, millel on aromaatne kuueliikmeline tsükkel ja mis on paljude valkude ja peptiidide ehitusplokk.
Lisaks mängib fenüülalaniin olulist rolli lämmastiku metabolismis ja seda saab muuta maksas proteinogeenseks aminohappeks türosiiniks. Fenüülalaniin ja türosiin mängivad olulist rolli insuliini, melaniini, türoksiini ja neurotransmitterite dopamiini, serotoniini ja türamiini sünteesis.
Mis on fenüülalaniin?
Fenüülalaniin on asendamatu alfa-aminohape, mis erinevalt enamikust proteinogeensetest aminohapetest ei ole mitte ainult L-kujul bioaktiivne, vaid piiratud määral ka R-vormi enantiomeer.
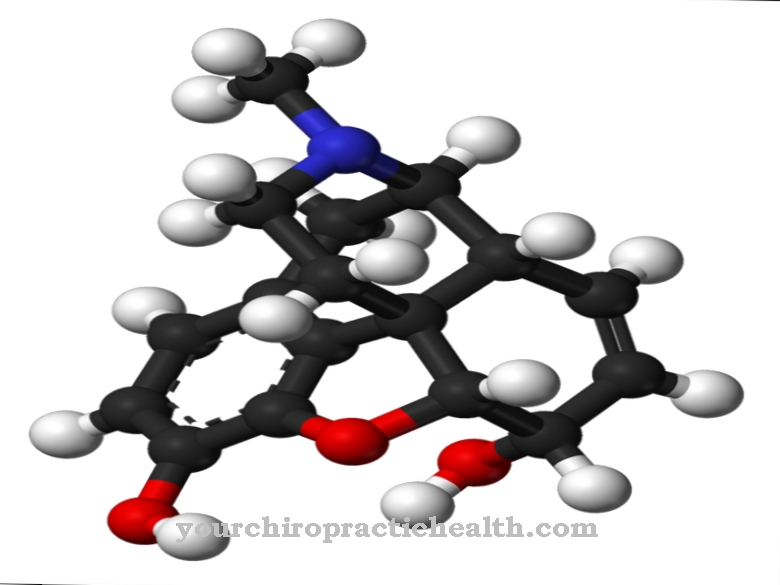
R-fenüülalaniin on biokeemiliselt suures osas passiivne ja toimub eranditult aminohappe kunstlikul tootmisel, kuid arutusel on D-fenüülalaniini roll valukompleksi teatud neurotransmitterite juhtimisel. Iseloomuliku struktuurina on fenüülalaniinil lihtne aromaatne kuueliikmeline tsükkel (benseenitsükkel) koos kinnitatud süsivesinikahelaga. Keemiline struktuurvalem on C6H5-CH2-CH (NH2) -COOH, kusjuures C6H5 rühm näitab benseenitsüklit. Aminohape on amfifiilne, mis tähendab, et see on nii rasvas kui vees lahustuv.
Keemiline valem näitab ka seda, et fenüülalaniin koosneb ainult süsinikust, vesinikust, lämmastikust ja hapnikust - ainetest, mis on kõikjal levinud. Haruldased metallid, mineraalid või mikroelemendid ei kuulu aminohapet. Sellegipoolest ei suuda inimese metabolism metaboliidi fenülalaniini sünteesida piisavas koguses türosiinist, vaid see sõltub toidu tarbimisest. Fenüülalaniini on paljudes loomsetes ja ka taimses toitudes piisavas koguses, nii et normaalse segatud toitumisega - eeldades seedetraktis normaalset imendumist - ei ole vaja karta aminohapet.
Funktsioon, mõju ja ülesanded
Fenüülalaniini kõige olulisem funktsioon ja ülesanne on osalemine paljude valkude ja peptiidide struktuuris. Samuti osaleb see mõnede hormoonide sünteesis, millel on keskne roll metaboolsete protsesside juhtimisel.
Seal on hormoone nagu adrenaliin, norepinefriin, L-dopa, PEA ja melaniin. Lisaks on L-fenüülalaniin põhiainena, millest z. B. sünteesida saabuvat ainet dopamiini, serotoniini, türamiini ja teisi. L-fenüülalaniin on ka asendamatu aminohappe türosiini lähtematerjal. Selleks muundatakse fenüülalaniin maksas kahes etapis hüdroksüülimise ja veemolekuli tükeldamise teel türosiiniks. Fenüülalaniini hüdroksülaas on ensüüm, mis katalüüsib muundumist türosiiniks.
Asendamatu aminohappe türosiini alternatiivne tarnimine võib toimuda toidu kaudu, nagu fenüülalaniini puhul. Vastupidiselt kõigile teistele aminohapetele, millel on ainult L-kujul bioaktiivsed toimed, näib fenüülalaniini D-enantiomeer vähemalt valu tajumist mõjutavat. L- ja D-fenüülalaniini segul (ratseemiline segu) leiti valuvaigistavat toimet. DL-segu blokeerib tõenäoliselt enkefaliinide - keha enda opioidide - lagunemise, nii et valuvaigistav toime püsib ja tugevneb.
Haridus, esinemine, omadused ja optimaalsed väärtused
Asendamatu aminohape fenüülalaniin imendub toidu kaudu. See ei ole vaba, kuid tavaliselt keemiliselt seotud kujul oleva valgu või polüpeptiidi osana. Aminohappe metabolismi jaoks kättesaadavaks tegemiseks tuleb vastav valk kõigepealt lagundada ja seejärel ekstraheerida "fragmentidest", kasutades edasises metabolismis ensüüme.
L-fenüülalaniini sünteesitakse niinimetatud sikimiinhappe teel. See on keeruline biokatalüütiline ahelreaktsioon, mis autotroofsetel taimedel ja bakteritel on. Autotroofsete organismide eripära on nende võime moodustada orgaanilisi aineid ainult anorgaanilistest materjalidest. Vaba L-fenüülalaniin maitseb mõrult, samas kui eranditult tööstuslikus tootmises toodetav D-enantiomeer on magusa maitsega. Aminohape on z. B. pakutakse toidulisandina ja kuulub ka kunstliku magusaine aspartaami hulka. Biosaadavat L-fenüülalaniini leidub seotud kujul paljudes toitudes.
Nende sisaldus on eriti kõrge kuivatatud hernestes ja sojaubades, kreeka pähklites ja kõrvitsaseemnetes ning erinevat tüüpi kalades ja lihades. Fenüülalaniini vajadus sõltub suuresti türosiini pakkumisest. Kui dieedis pole türosiini, vajab keha 38–52 mg 1 kg kehamassi kohta. Kuna dieedis on palju türosiini, langeb päevane vajadus ainult 9 mg-ni kehamassi kilogrammi kohta. Reeglina sisaldavad fenüülalaniini sisaldavad toidud ka vastavas koguses türosiini.
FAO / WHO 1985. aasta soovitus on L-fenüülalaniini ja L-türosiini liitvajadus 14 mg kehamassi kilogrammi kohta päevas. Seetõttu vajab täiskasvanu, kelle kehakaal on 80 kg, päevas mõlemat ainet 1120 mg.
Haigused ja häired
Puudulikkuse sümptomid fenüülalaniini ja türosiini püsivalt ebapiisava varustamise korral dieedis on äärmiselt haruldased, kuid neil võivad olla tõsised tagajärjed, eriti neuronite piirkonnas.
Lisaks paljude hormoonide ja neurotransmitterite sünteesi kahjustusele võib puudus ilmneda ka närvikiudude müeliniseerimise häirete tõttu. Puudujäägi vastand, fenüülalaniini (fenüülketonuuria) ülekontsentratsioon võib tekkida geneetilise metaboolse häire tõttu. Haigus päritakse autosomaalselt retsessiivsel viisil ja see põhjustab ensüümi fenüülalaniini hüdroksülaasi vähenenud tootmist, mis võib muuta fenüülalaniini türosiiniks.
Ensüümi vähenenud aktiivsus põhjustab aminohappe järsu suurenemise, mida nimetatakse fenüülketonuuriaks, kuna muundamine türosiiniks on ka fenüülalaniini lagunemistee. Samal ajal on puudu türosiin, kuna sünteesi tee on blokeeritud. Teine pärilik haigus selles kontekstis on Hartnupi sündroom. See on ainevahetushäire, mis häirib fenüülalaniini transporti läbi rakumembraani. See põhjustab tõsiseid probleeme kesknärvisüsteemis, nahas ja seedetraktis.

.jpg)







.jpg)
.jpg)